治験・臨床試験・臨床研究の支援を通じて
医療のエビデンス確立に貢献します。

TRIの支援は、基礎研究、非臨床試験、臨床試験、実用化まで多岐にわたります。
これまでの治験・臨床試験・臨床研究の支援によって蓄積したノウハウを最大限に活用し、研究デザインに応じた最適な支援を提案するとともに、プロジェクトマネジャーを中心に、専門家がチームを結成します。
スピード・コスト・クオリティを重視した最大価値の創出をワンストップで実現します。
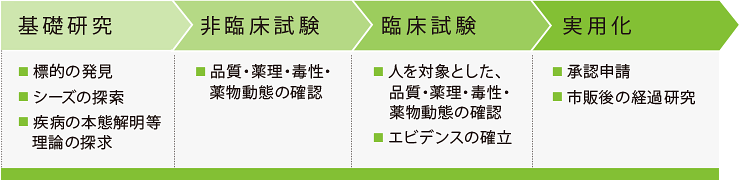
TRI支援の特長
- 綿密かつ周到なプロトコルの整備
- 目的に応じたデータ品質の確保
- 臨床研究データの専門的な解析
- 強固なネットワーク・サーバー環境
- 研究を管理・推進するための各種ITシステムの充実
- オピニオンリーダー医師および医師グループとの連携
- 大学や医療施設との契約のインフラ
- グローバル臨床試験の企画・立ち上げ・運営支援
支援フロー
日本発の医薬品を創出すべく、臨床研究・臨床試験や医師主導治験の支援を行うとともに国際展開も視野に入れ、スピーディな対応を目指しています。
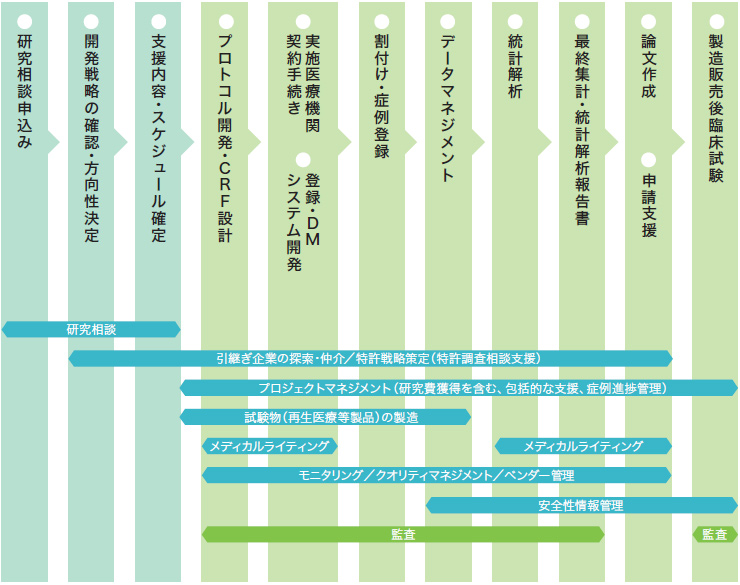
支援の申込
TRIによる支援をご希望いただく場合には研究相談にて内容をお伺いしております。まずは研究相談のお申込みをお願い致します。
TRIの業務について
- TRIが支援する研究の標準的な業務については以下をご覧ください。
支援内容の合意形成
研究相談にて研究内容やご要望等をお伺いし、受入れキャパシティや資金源等も含め検討の上、ご要望に最大限お応えできる支援内容を提案させていただきます。ご相談の上、最適な支援内容となるように調整いたします。
お問い合わせ先
(公益)神戸医療産業都市推進機構 医療イノベーション推進センター
〒650-0047 神戸市中央区港島南町1丁目5番地4号
Tel:078-303-9093
Fax:078-303-9094
E-mail: お問い合わせは こちら
〒650-0047 神戸市中央区港島南町1丁目5番地4号
Tel:078-303-9093
Fax:078-303-9094
E-mail: お問い合わせは こちら
